Investigadores del Centro de Biología Molecular “Severo Ochoa” (CBMSO), la Universidad Autónoma de Madrid (UAM) y el Hospital Universitario de Alcorcón han identificado un posible papel clave de la activación glial y la inflamación en la neurodegeneración del cerebelo de ratones que imitan la ataxia de Friedreich, una enfermedad neurodegenerativa hereditaria
La ataxia de Friedreich es una enfermedad hereditaria causada por una deficiencia de frataxina, una proteína clave para el funcionamiento de las mitocondrias, que son las encargadas de generar energía y regular el metabolismo celular. Esta deficiencia se debe a una mutación genética, en la mayoría de los casos por una expansión anómala de un triplete GAA en el ADN, que puede repetirse de 70 a más de 1.500 veces. Los síntomas suelen aparecer entre los 3 y 20 años y se manifiesta, entre otros signos, con la pérdida de coordinación motora, resultado de la degeneración de la médula espinal y el cerebelo.
Ahora, un equipo liderado por el Dr. Javier Díaz-Nido (Centro de Biología Molecular “Severo Ochoa” y Universidad Autónoma de Madrid), y por la Dra. Frida Loría (Hospital Universitario de Alcorcón), ha caracterizado el proceso neurodegenerativo de esta enfermedad en una cepa de ratones modificados genéticamente.
Esta cepa, denominada YG8-800, fue diseñada eliminando el gen de la frataxina en ratones e introduciendo el gen humano con más de 800 repeticiones del triplete GAA. Estos ratones desarrollan progresivamente síntomas similares a la ataxia de Friedreich, con una pérdida severa de coordinación motora que se agrava con la edad.
El estudio, publicado en la revista Neurobiology of Disease, aporta información valiosa sobre los mecanismos moleculares implicados en la neurodegeneración de esta enfermedad, lo que podría conducir al descubrimiento de nuevas dianas terapéuticas. Además, establece las bases para la investigación de posibles terapias que frenen la progresión de la enfermedad.
Activación temprana de las células gliales
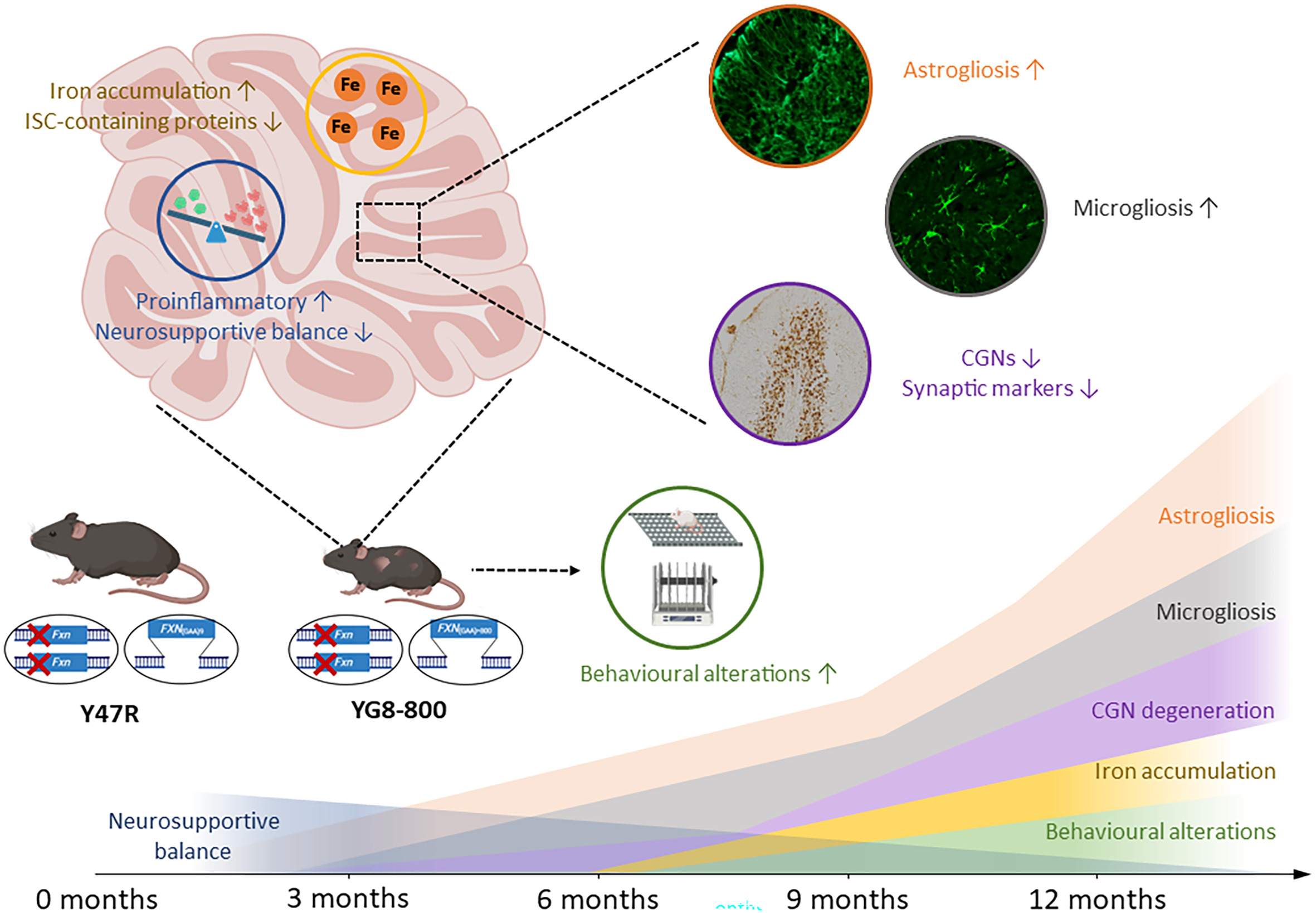
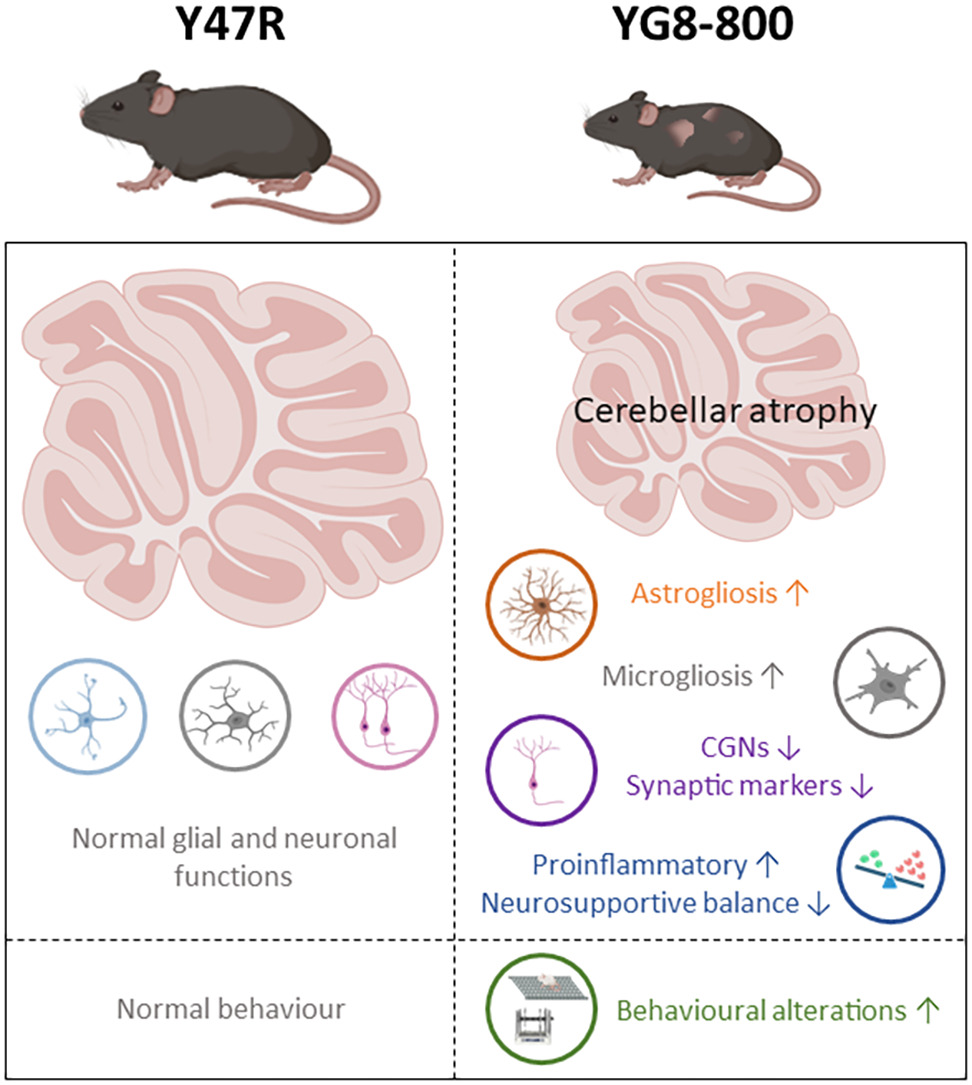
El análisis detallado de los ratones YG8-800 mostró a los científicos una atrofia progresiva del cerebelo, asociada a la degeneración de las neuronas granulares en la corteza cerebelosa. A nivel molecular, los bajos niveles de frataxina se correlacionan con niveles bajos de proteínas de la cadena transportadora de electrones mitocondrial y con una acumulación de hierro en el cerebelo.
“Todo ello apunta al posible papel de la disfunción mitocondrial y al estrés oxidativo como factores conducentes a la degeneración de las neuronas”, afirman los autores.
“Curiosamente —agregan—, antes de detectar ningún signo evidente de degeneración neuronal, observamos la presencia de astrocitos reactivos y células de microglía activada en la corteza cerebelosa de los ratones YG8-800, que es detectable ya a los 3 meses de edad”.
Esta activación temprana de las células gliales está asociada a un aumento en la expresión de citoquinas proinflamatorias. Además, los autores detectaron una alteración en los factores neurotróficos, esenciales para la supervivencia de las neuronas. “En el caso del Factor Neurotrófico Derivado del Cerebro (BDNF), observamos un incremento de su expresión a los 3 meses de edad y una marcada reducción a partir de los 6 meses”.
Estos hallazgos sugieren, en suma, que tanto la neuroinflamación como la reducción de factores neurotróficos podrían contribuir a la neurodegeneración en el cerebelo de los ratones YG8-800.
Referencia bibliográfica: Vicente-Acosta A, Herranz-Martín S, Pazos MR, Galán-Cruz J, Amores M, Loria F, Díaz-Nido J. Glial cell activation precedes neurodegeneration in the cerebellar cortex of the YG8-800 murine model of Friedreich ataxia. Neurobiol Dis. 2024 Oct 1;200:106631. doi: 10.1016/j.nbd.2024.106631. Epub 2024 Aug 5. PMID: 39111701.
Fotografía de portada: M. Richter/Pixabay.

