Investigadores de la <a href="https://www.uam.es/uam/inicio?language=es" title="Universidad Autónoma de Madrid" alt="Universidad Autónoma de Madrid" target="_blank">Universidad Autónoma de Madrid</a> (UAM) han descubierto que los aminoácidos se enlazan en fase gas formando estructuras moleculares muy complejas. La extraordinaria estabilidad de estas estructuras se debe principalmente a los enlaces de hidrógeno que se establecen entre ellas.
Un reciente estudio, publicado en la revista Physical Chemistry Chemical Physics, y llevado a cabo por investigadores del Departamento de Química de la Universidad Autónoma de Madrid (UAM), el Instituto de Física de la Materia Condensada (IFIMAC) y el Instituto de Química Avanzada (IAdChem), aporta información fundamental sobre las interacciones entre aminoácidos en agregados moleculares antes de formar las cadenas polipeptídicas.
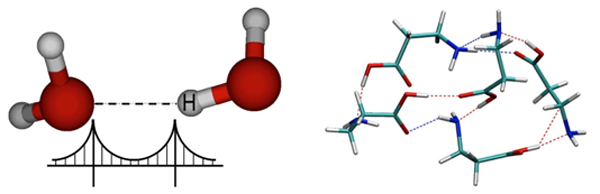
Izquierda: dos moléculas de agua conectadas por un enlace puente de hidrógeno. Derecha: ejemplo de una de las estructuras descubiertas. Se trata de un agregado formado por cinco moléculas del aminoácido β-alanina, conectadas por diversos puentes de hidrógeno. / UAM
Concretamente, los investigadores han estudiado las fuerzas que mantienen unidos agregados formados por moléculas de β-alanina, un aminoácido lineal presente en los tejidos musculares y cerebrales (formando parte de los péptidos carosina y anserina) y en nutrientes esenciales como la vitamina B5 o ácido pantoténico.
Para entender dichas interacciones y conocer más sobre las propiedades de las moléculas, los investigadores realizaron simulaciones mediante cálculos basados en mecánica cuántica. Estas simulaciones, altamente costosas en términos de tiempo y recursos de computación, fueron realizadas en el Centro de Computación Científica de la Universidad Autónoma de Madrid (CCC-UAM).
Los investigadores estudiaron así más de ochenta estructuras formadas por dos, tres, cuatro y cinco moléculas de β-alanina en fase gas, seleccionando las más estables para la evaluación de sus propiedades. En concreto, valoraron en detalle las interacciones mediante puentes de hidrógeno implicadas en su estructura. La importancia de estas interacciones, radica en la extraordinaria estabilidad que les confiere a estos complejos sistemas moleculares.
"En la naturaleza, el átomo de hidrógeno es el más sencillo y abundante en el universo, y juega un papel fundamental, siendo capaz de mantener unidas moléculas tan complejas como los aminoácidos", indica Dariusz G. Piekarski, estudiante de doctorado del Departamento de Química de la UAM y autor principal del trabajo.
LOS AMINOÁCIDOS Y LOS PUENTES DE HIDRÓGENO
Los aminoácidos son moléculas orgánicas fundamentales para la vida. Los más habituales son los que se encuentran en los péptidos y proteínas. La formación de péptidos y proteínas ocurre a través de una reacción química en la que dos aminoácidos interaccionan liberando una molécula de agua y formando un enlace peptídico. Un tercer aminoácido puede a su vez interaccionar por un extremo de la molécula formando un nuevo enlace peptídico, y así se enlazan formando cadenas.
Sin embargo, los aminoácidos pueden además establecer otro tipo de fuerzas de unión intermoleculares. Las fuerzas de interacción entre moléculas, son de carácter electrostático y se denominan fuerzas de Van der Waals. Estas fuerzas se caracterizan por ser muy débiles comparadas con el enlace químico.
Un tipo de interacción entre moléculas con un carácter muy particular es el enlace de hidrógeno, también denominado ‘enlace por puente de hidrógeno’. Estas fuerzas de unión tienen lugar entre un átomo de hidrógeno enlazado químicamente a una molécula, e interactuando electrostáticamente con otra molécula.
Los enlaces de hidrógeno son esenciales para la vida. Son, por ejemplo, los principales responsables de la unión entre moléculas de agua, confiriéndole sus conocidas propiedades macroscópicas. También son los responsables de la estabilidad en la unión de las dos hélices de la estructura del ADN. De forma análoga, en las proteínas una vez formados los enlaces peptídicos, las cadenas se estabilizan mediante puentes de hidrógeno formados entre ellas, confiriéndoles estructura tridimensional.
"En el futuro planeamos extender nuestros estudios evaluando cómo reaccionan los agregados moleculares de aminoácidos frente a radiaciones ionizantes. Para ello estamos trabajando en colaboración con colegas de la Universidad de Caen - Normandía (Francia) y el Consiglio Nazionale delle Richerche (CNR, Italia), expertos en irradiar moléculas en aceleradores de partículas. Podremos así estudiar su estabilidad y evolución frente a este tipo de radiación", detalla Sergio Díaz-Tendero, investigador Ramón y Cajal del Departamento de Química de la UAM, el IFIMAC y el IAdChem, codirector de la tesis de Dariusz G. Piekarski.
Referencia bibliográfica:
Structure and stability of clusters of β-alanine in the gas phase: importance of the nature of intermolecular interactions. Dariusz G. Piekarski and Sergio Díaz-Tendero, Phys.Chem. Chem. Phys. 19, 5465(2017). DOI: 10.1039/c6cp07792g

