Un equipo español con amplia experiencia en el desarrollo de tecnologías útiles para la industria alimentaria, y que es liderado desde la <a href="https://www.uam.es/uam/inicio?language=es" title="Universidad Autónoma de Madrid" alt="Universidad Autónoma de Madrid" target="blank">Universidad Autónoma de Madrid</a> (UAM), ha conseguido ahora diseñar un biosensor que abarata tiempo y recursos en la detección de ácido láctico en alimentos tan diferentes como vino, cerveza y yogur.
El grupo de investigación Sensores químicos y biosensores del Instituto de Investigación Avanzada en Química de la Universidad Autónoma de Madrid (UAM) y el Instituto IMDEA Nanociencia ha desarrollado un biosensor que, de forma rápida y directa, logra detectar en vino, cerveza y yogur ácido láctico, sustancia que afecta el sabor y la calidad de los alimentos.
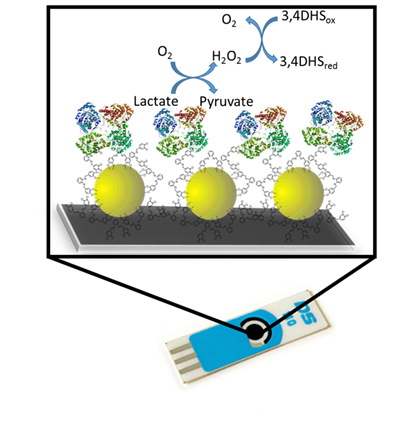
Esquema del nuevo biosensor de lactato
El biosensor supone una gran ventaja en la industria alimentaria. Permite la determinación de hasta 2,6 x10-6 moles/litro de lactato directamente, sin ningún tratamiento previo de la muestra.
"Los resultados son similares a los obtenidos usando un kit de ensayo enzimático estándar, con la ventaja de que la determinación de lactato con el sensor es mucho más rápida y económica", afirman los investigadores.
ASÍ FUNCIONA
El dispositivo se ha desarrollado mediante inmovilización de lactato oxidasa sobre nanopartículas de oro, obtenidas por reducción de la sal de oro (tetracloroaurato de hidrógeno trihidratado) con un ligando tetradentado de base de Schiff, concretamente el N,N'-Bis (3,4-dihidroxibencilideno)-1,2-diaminobenceno) indicado como 3,4-DHS, que tras la reducción recubre a las nanopartículas obtenidas evitando su agregación.
El bioconjugado nanopartícula-enzima resultante se ha depositado, a su vez, sobre electrodos serigrafiados de carbono desechables. El ligando, además de su acción de reducción, proporciona un recubrimiento robusto a las nanopartículas de oro y una función catalítica, reduciendo el potencial de oxidación del peróxido de hidrógeno a +0.2 voltios, lo que evita posibles interferencias por parte de otros compuestos presentes en la muestra que se oxidarán a potenciales más altos.
Cuando el biosensor se introduce en una muestra que contiene lactato, la lactato oxidasa cataliza la conversión de L-lactato en piruvato en presencia de oxígeno, produciendo peróxido de hidrógeno, que se oxida catalíticamente en el electrodo. La corriente catalítica medida es directamente proporcional a la concentración de peróxido, que está directamente relacionada con la cantidad de lactato presente en la muestra.
Referencia bibliográfica:
Bravo I, Revenga-Parra M, Pariente F, Lorenzo E. Reagent-Less and Robust Biosensor for Direct Determination of Lactate in Food Samples. Sensors. Doi: 10.3390/s17010144.

